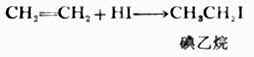|
第二节 烯烃 一、烯烃的构造和通式 烯烃是指一类含有碳碳双键( 此它又称为不饱和烯。根据碳碳双键的数目,烯烃又可以分为单烯烃(含一个双键)、二烯烃(含两个双键)和多烯烃(含多个双键)。其中以单烯烃和共轭二烯烃最为重要。平时“烯烃”这个名字是代表单烯烃的意思,所以通常烯烃是指含有一个碳碳双键的不饱和烃而言。烯烃的通式是CnH2n。碳碳双键( 烯烃的碳碳双键( 二、烯烃的同分异构现象 (一)构造异构 由于存在双键,使烯烃的异构体数目比相应的烷烃多。如丁烷只有两种同分异构体,而分子式为C4H8的丁烯则有三种构造异构体。
(二)顺反异构 除上述两种异构现象外,由于以双键相连的两个碳原子不能绕σ键轴自由旋转,所以当两个碳原子上各连有两个不同的原子或基团时(如2-丁烯),双键上的四个基团在空间就可以有两种不同的排列方式,即两种构型。
顺反异构体是两种不同的化合物。顺反异构体不仅在理化性质上不同,它们的生理活性也往往有差异,如具有降血脂作用的亚油酸,它的两个双键都是顺式构型。
三、烯烃的命名法 烯烃的系统命名法的关键也是如何选择母体化合物和如何确定取代基的位置。 1.选择含有双键的最长碳链为主链作为母体。主链上的碳原子从靠近双键的一端开始编号,并把双键位置写在烯烃名称的前面。
烯烃去掉一个氢原子生成一价基团,叫做烯基。碳链的编号应从含有自由键的碳原子开始。例如:
(1) 将各种取代基的原子(与C=C的碳相连的原子)按原子序数大小排列,大者为“较优”基团。例如:I>Br>Cl>S>P>O>N>C>H(“>”表示“优于”)。 (CH3)2C->(CH3)2CH->CH3CH2->CH3- 假使第二个原子也相同时,则沿取代链逐次相比。例如:
此外应注意:一个原子序数大的原子要比两个或三个原子数小的原子优先,例如: -CH2CL>-C(CH3)3 因此,此规则是比较原子序数的大小,而不是几个原子的原子序数之和。 (3)有双键或三键的基团:
时,叫做Z型(Z取自德文Zusammen,在一起);当a与c在参考平面两侧时,叫做E型(E取自德文Entgegen,相反,相对)。Z,E写在括号里,放在化合物系统名称的前面。
例1
例2
四、烯烃的物理性质 烯烃的物理性质如熔点、沸点、相对密度和溶解度等与相应的烷烃相似。常温时,C2~C4的烯烃是气体,C5~C18是液体,C18以上是固体。烯烃都难溶于水而易溶于有机溶剂。 表11-4 烯烃的物理常数
碳原子数 构造式 熔点/℃ 沸点/℃ 相对密度(d204) 2 H2C=CH2 -169 -102
3 CH3CH=CH2 -185 -48
4 CH3CH2CH=CH2 -185 -6.5 0.5946 5 CH3(CH2)2CH=CH2 -138 29 0.6411 6 CH3(CH2)3CH=CH2 -138 63 0.6734 8 CH3(CH2)5CH=CH2 -101 121 0.7149 10 CH3(CH2)7CH=CH2 -66 170 0.7408 12 CH3(CH2)9CH=CH2 -35 213 0.7584 14 CH3(CH2)11CH=CH2 -12 246 0.7852 18 CH3(CH2)15CH=CH2 17
0.7891 20 CH3(CH2)17CH=CH2 28 341 0.7882 五、烯烃的化学性质 烯烃的官能团是 与碳原子的结合不很牢固。由于烯烃具有易断裂和易极化的不稳定的π键,故使它具有不同于烷烃的特殊化学性质,如易发生加成、氧化、聚合等反应。 (一)加成反应 烯烃的加成反应是指在起反应时,烯烃分子中π键断裂,试剂中的两个原子或原子团分别加到双键的两个碳原子上的反应。双键加成的典型反应可表示为:
1.加氢 在普通情况下,烯烃与氢并不发生反应。如有适当的催化剂(Pt,Pd,Ni)存在,烯烃在液相或气相下能够氢化,变成相应的烷烃。例如:
这种在催化剂作用下的加氢反应,称为催化氢化。由于催化氢化反应可以定量地进行,所以可根据吸收量的计算来分析样品中双键的数目。 2.加卤素 烯烃与卤素(氯或溴)加成反应是亲电加成反应,这个反应在常温下就能很迅速地发生,例如:
3.加卤化氢 烯烃与卤化氢(HI,HBr,HCl)的加成反应也是亲电加成反应,生成卤代烷。例如:
对HX一类试剂,加在双键上的两部分(H与X)不一样,所以叫做不对称试剂。乙烯是对称烯烃,它和不对称试剂加成产物只有一种。若不对称试剂和不对称烯烃发生加成反应时,加成方式就有两种可能,例如,丙烯与氯化氢加成时,产物可能是: (责任编辑:泉水) |
第二节 烯烃
时间:2006-07-01 21:43来源:大众医药网 作者:admin 点击:
322次
顶一下
(5)
100%
踩一下
(0)
0%
------分隔线----------------------------
- 发表评论
-
- 最新评论 进入详细评论页>>
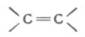 烯烃分子中不是所有碳原子的价都饱和了,因
烯烃分子中不是所有碳原子的价都饱和了,因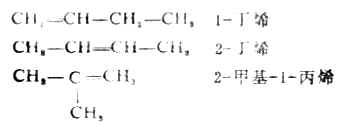 在烯烃的构造异构体中,有一种是碳链异构,即骨架不同的异构现象。如1-丁烯(或2-丁烯)与2-甲基-1-丙烯;另一种是由于双键的位置不同,如1-丁烯和2-丁烯。这种由于官能团位置的不同而产生的异构现象叫做位置异构。碳链异构与位置异构都属于构造异构。
在烯烃的构造异构体中,有一种是碳链异构,即骨架不同的异构现象。如1-丁烯(或2-丁烯)与2-甲基-1-丙烯;另一种是由于双键的位置不同,如1-丁烯和2-丁烯。这种由于官能团位置的不同而产生的异构现象叫做位置异构。碳链异构与位置异构都属于构造异构。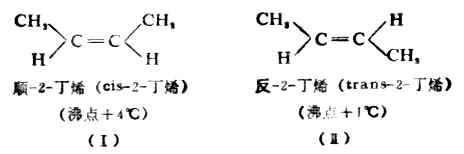 这两个异构体在原子或基团的连接顺序及官能团的位置上均无区别,即构造相同;它们的区别仅在于基团在空间的排列方式不同。在前一个化合物(Ⅰ)中,相同的基团(两个甲基或两个氢原子)在双键的同侧,叫做顺式异构体(词头cis-系拉丁字,意指在一边),而后者(Ⅱ)的两个甲基(或两个氢原子)则在双键的两侧,所以叫做反式异构体(词头trans-系拉丁字,意指交叉)。这种异构现象叫做顺反异构,是立体异构的一种,属于构型异构。立体异构是构造相同,但分子中的原子或原子团在空间排布不同的同分异构现象。构型异构是立体异构中的一种,是构造相同,构型不同的立体异构现象。
这两个异构体在原子或基团的连接顺序及官能团的位置上均无区别,即构造相同;它们的区别仅在于基团在空间的排列方式不同。在前一个化合物(Ⅰ)中,相同的基团(两个甲基或两个氢原子)在双键的同侧,叫做顺式异构体(词头cis-系拉丁字,意指在一边),而后者(Ⅱ)的两个甲基(或两个氢原子)则在双键的两侧,所以叫做反式异构体(词头trans-系拉丁字,意指交叉)。这种异构现象叫做顺反异构,是立体异构的一种,属于构型异构。立体异构是构造相同,但分子中的原子或原子团在空间排布不同的同分异构现象。构型异构是立体异构中的一种,是构造相同,构型不同的立体异构现象。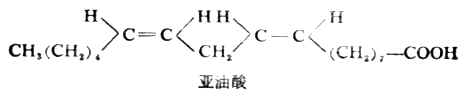
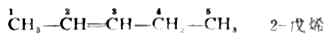 2.把支链作为取代基,其位置、数目和名称按“次序规则”(见后)“较优”者后列出的顺序写在某烯之前。
2.把支链作为取代基,其位置、数目和名称按“次序规则”(见后)“较优”者后列出的顺序写在某烯之前。
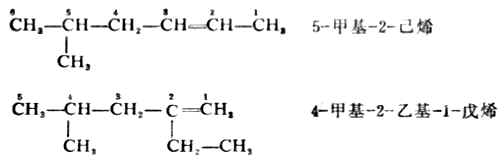 3.如双键在主链的中央,则编号从靠近取代基的一端开始。
3.如双键在主链的中央,则编号从靠近取代基的一端开始。
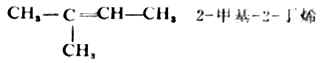 4.烯烃主链上的碳原子在十个以上时,烯字的前面应加一个“碳”字。
4.烯烃主链上的碳原子在十个以上时,烯字的前面应加一个“碳”字。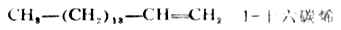
 5.对于双键碳原子上连结有四个不同取代基的烯烃,其顺反异构体如用相同基团在双键的同侧或异侧的方法命名则遇到困难,例如:
5.对于双键碳原子上连结有四个不同取代基的烯烃,其顺反异构体如用相同基团在双键的同侧或异侧的方法命名则遇到困难,例如:
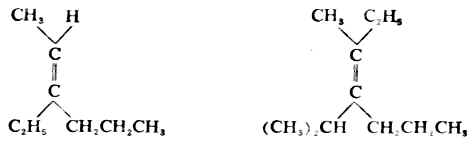 这时应根据Cahn-Ingold-Prelog的顺序规则对顺反异构体命名。次序规则是为了表达某些立体化学关系,须决定有关原子或原子团的排列次序时所用的方法。其主要内容如下:
这时应根据Cahn-Ingold-Prelog的顺序规则对顺反异构体命名。次序规则是为了表达某些立体化学关系,须决定有关原子或原子团的排列次序时所用的方法。其主要内容如下:
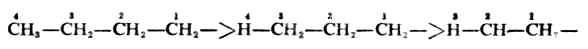
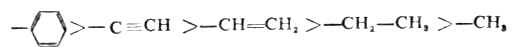 根据上述规则,一此常见的原子及原子团的优先顺序是:I>Br>Cl>-SO3H>F>
根据上述规则,一此常见的原子及原子团的优先顺序是:I>Br>Cl>-SO3H>F>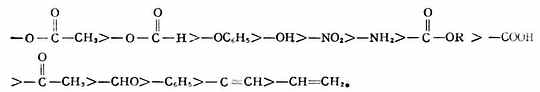 按次序规则决定双键上每个碳所连的两个原子或原子团的优先次序后,在下式中,如a>b,c>d,则当a与c在参考平面(π键所在平面,即与
按次序规则决定双键上每个碳所连的两个原子或原子团的优先次序后,在下式中,如a>b,c>d,则当a与c在参考平面(π键所在平面,即与 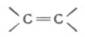 平面相垂直的平面)同侧
平面相垂直的平面)同侧
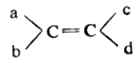
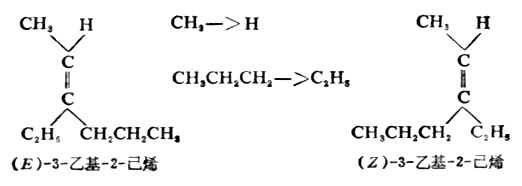
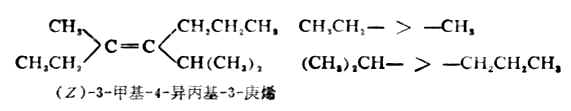
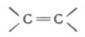 。π电子云成块状分布于五个σ键所在平面的上下两侧,它
。π电子云成块状分布于五个σ键所在平面的上下两侧,它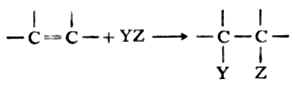

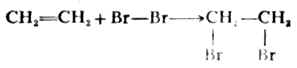 如果用溴的四氯化碳溶液时,反应结束后溴的棕红色消失。常用这个方法来鉴定化合物是否含有碳碳双键。
如果用溴的四氯化碳溶液时,反应结束后溴的棕红色消失。常用这个方法来鉴定化合物是否含有碳碳双键。