|
7月3日,《自然》在线发表了中科院上海巴斯德研究所江陆斌研究组的最新研究成果,首次发现了恶性疟原虫在人体内实现免疫逃逸的表观遗传分子机制,并为研制新型疟疾疫苗提供了实验基础。针对该研究结果,《自然》于7月3日专设“疟疾论坛”板块进行了讨论。来自美国Stowers医学研究所的Jerry Workman博士与来自瑞典卡罗琳学院的Mats Wahlgren博士指出:“该研究结果对人们更好地理解真核生物基因调控以及疟疾疫苗的研发所具有的科学意义”。
疟疾是一种主要的热带寄生虫病。由恶性疟原虫引发的恶性疟疾每年在全世界范围内造成至少100万人死亡、3-5亿人感病,是最严重的一种寄生虫病。由于当前并无有效的疟疾疫苗,新型疟疾疫苗的研发已成为世界医学健康领域的当务之急。
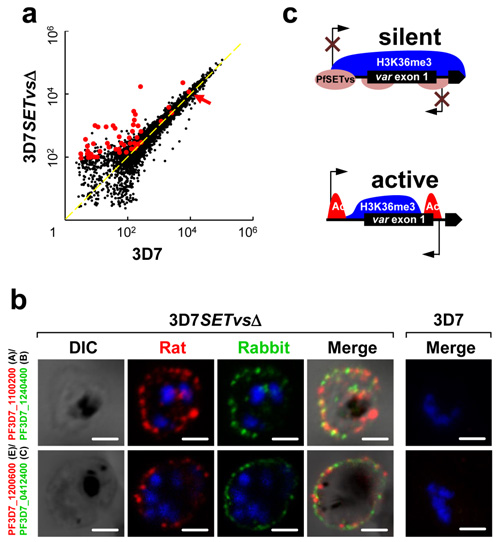
恶性疟原虫的基因组编码一个由60个基因组成的var基因家族。该基因家族的蛋白翻译产物PfEMP1在恶性疟原虫感染红细胞后可被运输至红细胞膜表面,是一种主要的寄生虫致病蛋白。人体针对PfEMP1蛋白产生的抗体可有效地抑制表达这种PfEMP1的恶性疟原虫在红细胞内的寄生。但由于单个恶性疟原虫在红细胞感染期内只能同时转录一个var基因,因此恶性疟原虫可利用var基因家族的这种相互排斥性表达机制成功地逃避人体针对PfEMP1产生的抗体反应。目前,关于var基因的这一转录调控机制尚不清楚。
通过实验研究,江陆斌研究组成功地找到了控制var基因沉默的关键因子PfSETvs。PfSETvs作为果蝇ASH1的同源蛋白,是一种组蛋白赖氨酸甲基化酶。研究人员证明,PfSETvs可在var基因的启动子区域产生一类特异性的组蛋白修饰H3K36me3,进而抑制var基因家族的转录。
这项研究首次证明了真核生物中组蛋白修饰H3K36me3对基因沉默的介导作用;研究中通过敲除PfSETvs基因产生的可表达全部PfEMP1蛋白的转基因恶性疟原虫株也为研制新型疟疾疫苗提供了实验基础。
该研究由江陆斌研究组联合美国国立卫生研究院、法国巴斯德所、同济大学、复旦大学及丹麦哥本哈根大学等多家研究单位共同完成,获得了国家自然科学基金(81271863)、中国科学院重点部署项目(KSZD-EW-Z-003-1-2)、美国国立卫生研究院内部研究基金及欧洲研究委员会专项基金PlasmoEscape(250320)的资助。 (责任编辑:泉水) |
上海巴斯德所等发现恶性疟原虫实现免疫逃逸的分子机制
时间:2013-07-12 10:49来源:上海巴斯德研究所 作者:未知 点击:
106次
顶一下
(0)
0%
踩一下
(0)
0%
------分隔线----------------------------
- 发表评论
-
- 最新评论 进入详细评论页>>
- 推荐内容
-
- 患有和不患有MS的妇女妊娠率和结局
近日,神经病学领域权威取杂志Neurology上发表了一篇研究文章,...
- 上海巴斯德所发现人体固有免疫系
11月21日,国际学术期刊JournalofHepatology在线发表了中国科学院上...
- 免疫治疗:未来值得关注的四大趋
2010年,美国FDA批准前列腺癌免疫治疗药sipuleucel-T用于临床,到现...
- 终止妊娠无痛不代表无害 年轻人存
原标题:终止妊娠无痛不代表无害 年轻人存在3类避孕误区 在大...
- 我武生物董事长回应默沙东舌下免
大智慧阿思达克通讯社4月23日讯,我武生物(300357.SZ)董事长胡...
- 武汉病毒所在T细胞的天然免疫性研
近来,中国科学院武汉病毒研究所唐宏课题组的系列研究表明,...
- 患有和不患有MS的妇女妊娠率和结局