|
你侬我侬,忒煞情多。情多处热如火。 把一块泥,捻一个你, 塑一个我,将咱两个, 一齐打破,用水调和, 再捻一个你,再塑一个我。 我泥中有你,你泥中有我……[1] 在传统文化中,合体似乎是一种情侣之间恩爱到极致的表现。不但中国如此,在希腊神话中,湖中水仙萨耳玛西斯(Salmacis)对赫马佛洛狄忒斯(Hermaphroditus)也爱得深沉,向天许愿要和他永远在一起。于是神满足了她的愿望,啪一下,这对异性恋就合体了,后来成为一个雌雄同体的神。于是,赫马佛洛狄忒斯的名字也就成了 “雌雄同体”(Hermaphrodite)一词的词源。 而在现代通俗文化中,合体已不仅仅是异性恋的专利了,从孙悟空贝吉塔到葫芦娃七兄弟,一经合体,战斗力瞬间飙升几个数量级,让电视机前的小朋友们个个热血沸腾,恨不得马上拉上个小伙伴去合体战斗。
那么,科学会允许我们“合体”吗? 自然发生的“合体”:非常罕见,“成品”极少显然,要想把两个大活人合体到一块,可不是揉揉碎混混匀再捏两下这么简单的。不过,如果把“合体”的范畴稍微拓宽一些,这事却也还有商量的余地。 在自然状态下,处于胚胎阶段的两个个体会有极其微小的几率“融合”到一起——最后,这两个胚胎的细胞会像充分混匀的红豆和绿豆一样难以分开,共同组成一个婴儿。 在希腊神话中,有一种由狮、蛇、羊三种动物彼此嵌合而成的怪物叫做喀迈拉(Chimera),早期的科学家们化用了这个典故,将这些由多个胚胎融合而成的个体也命名为“喀迈拉”。只不过,当初将它翻译成汉语的人似乎对神话并不感冒,直接将Chimera意译成了“嵌合体”。 自然发生的嵌合体非常罕见。不少情况下,胚胎融合诞生出的都是融合到一半的“半成品”,也就是我们常说的连体婴儿。由此看来,“合体”这种“不自然”的事情,交给大自然似乎也不是那么靠谱。 但是这类现象却深深地启发了科学家们,他们迅速意识到,尽管动物的成体不能直接融合,但是至少在胚胎发育的某个阶段里面,两个独立的胚胎存在水乳交融的可能性。对科学家们而言,“合体”不但是一个有趣的研究课题,更可能是一种研究动物胚胎发育机制的潜在手段。 有趣归有趣,但真的做起来,这就不那么简单了。不,应该说是困难重重才对: 一、黑白小鼠“合体”:未被重视的成功案例经过反复摸索,他们将“合体计划”锁定在了胚胎早期一个特殊的阶段——囊胚(Blastocyst)。
囊胚在结构上可以分为两个部分,一个是外围的“滋养外胚层”,另一个则是内部的“内细胞团”——这一团当中的细胞,便是大名鼎鼎的“胚胎干细胞”。组成我们身体器官的每一个细胞,都是这团胚胎干细胞的后代。 理论上讲,只要把来自两个囊胚的胚胎干细胞混到一起,就有可能弄出个嵌合体来。基于“人类未动,小鼠先行”这条生物学研究铁律,1968年,剑桥大学的生理学家加德纳(R. L. Gardner)首先将一只黑毛小鼠囊胚的内细胞团塞到了一只白毛小鼠的囊胚腔中[2]。 在发育的过程中,这两只老鼠的内细胞团融合到了一起,最后出生了一只黑白相间的“奶牛色”小鼠——这首次证明了人工制造嵌合体的可能性。只不过,在他那个年代,这种工作既缺乏实用价值,也没能如预想般加深太多对胚胎发育机制的理解,因而充其量只能算是科学家的自娱自乐,在学术界并未引起多少关注。
二、体外培养“合体”材料:嵌合体技术登台亮相的大前提1981年,那是干细胞学界的春天。那一年,剑桥大学的生物学家马丁·埃文斯爵士(Sir Martin John Evans)与马修·考夫曼(Matthew H. Kaufman)[3],和美国加州大学教授盖尔·马丁(Gail Roberta Martin)[4]几乎同时发明了小鼠胚胎干细胞的体外培养技术。
他们将小鼠的胚胎干细胞从囊胚中分离出来,培养在一类可以强烈抑制其分化的特殊培养体系中,使之永远维持在胚胎干细胞的状态。这些具有分化成所有体细胞潜能的细胞,从此不只是在囊胚中的昙花一现。 较之成熟的动物个体,体外培养的细胞更容易实现各种基因编辑,同时又具备着分化成所有类型体细胞的潜力。因此,立刻有人意识到,这很可能带来一场的制造基因编辑动物的技术革命。 但是,光有胚胎干细胞是没法直接产生动物个体的。怎么才能把养在盘子里的胚胎干细胞。变成养在笼子里活蹦乱跳的实验动物呢?这时候,埃文斯爵士注意到了加德纳“奶牛色小鼠”。 他尝试在体外培养的胚胎干细胞直接注射到囊胚腔,结果很幸运地发现,和加德纳在囊胚中混合的内细胞团一样,体外培养的胚胎干细胞可以参与形成嵌合体。
三、哺乳动物接连“合体”:进程卡在灵长类上从那以后,新世界的大门被打开了。埃文斯发明的囊胚注射胚胎干细胞技术简单高效,经过后人的改进并臻于成熟后,时至今日都是制造基因编辑动物的主要手段之一。作为胚胎干细胞学的奠基人,埃文斯爵士也由于这项划时代的成就而获得了2007年诺贝尔生理或医学奖[5]。 一时间,冒险家们蜂拥而至。 十几年间,大鼠、兔子以及各种家畜的胚胎干细胞也相继实现了体外培养。作为制作基因编辑动物的核心技术,嵌合体技术在科研、畜牧等领域的作用变得举足轻重。从某种意义上说,20世纪的八九十年代,正是嵌合体技术发展得如火如荼的盛夏。 但在这一片繁荣之上,却飘着一朵令人不安的乌云。 与小鼠的巨大成功形成鲜明对比的是,包括人类在内的灵长类胚胎干细胞却始终不能在体外培养。 四、灵长类胚胎干细胞体外培养:千呼万唤始出来灵长类胚胎干细胞在生物医学研究中的重要性不言而喻。然而,灵长类胚胎干细胞研究不但难度大到令人发指,而且还总是面临着毫不留情的伦理争议,堪称是干细胞学领域的第一大坑,折磨着一代又一代干细胞学家。 好在功夫不负有心人,经过多年求索,美国发育生物学家詹姆斯·汤姆森(James A. Thomson)终于为这个大坑迎来生机:1997年,他成功体外培养了四株猕猴的胚胎干细胞[6],次年他又实现了人类胚胎干细胞的体外培养[7]。
灵长类人工嵌合体的诞生终于近在咫尺了。 五、灵长类“合体”:世纪末的沉重打击真的近在咫尺了? 并没有。 出乎所有人的预料,尽管汤姆森从灵长类囊胚中分离培养的肯定是胚胎干细胞无误,但是这些胚胎干细胞竟完全无法参与形成灵长类的嵌合体。这个让人崩溃的结果告诉科学家们,干细胞学领域的第一大坑依然还跟以前一样深不见底。 更无奈的是,就在汤姆森实现这项令人丧气的重大突破之时,命运女神仿佛也已经决定弃嵌合体技术而去了。 1997年,那是嵌合体技术肃杀的秋天。那一年,一只名叫“多莉”的绵羊在苏格兰呱呱坠地,伴随它的诞生,一种叫做“克隆”的崭新技术在干细胞领域冉冉升起。有了克隆技术,人们完全可以一步到位地制造出“纯而又纯”的动物。反观嵌合体,再怎么样制造出来的也是多个胚胎“合体”产生的“杂种”。随着越来越多种动物被成功克隆,嵌合体制造技术逐渐开始退居二线。 前有令人毫无头绪的技术瓶颈,后有新生代技术的步步进逼,灵长类嵌合体这条道路,在20世纪的末章,眼看着就要步入死地。 究竟是从此一蹶不振,还是会绝境逢生?在众人的困惑与迷茫中,嵌合体技术的凛冬将至了…… (编辑:Calo) 灵长类的胚胎“合体”之路有没有走进死胡同?嵌合体技术又将走向何方?在《你知道在生物学界,“求合体”有多难吗!(下)》中,文章里的故事将追上现实的进度条,敬请期待。 参考资料:
文章题图:thisisinfamous.com(责任编辑:泉水) |
你知道在生物学界,“求合体”有多难吗!(上)
时间:2015-09-24 21:43来源:果壳网 作者:鬼谷藏龙 点击:
221次
顶一下
(0)
0%
踩一下
(0)
0%
------分隔线----------------------------
- 上一篇:火星和泰坦上的生命,可能会是什么模样?
- 下一篇:核桃盘了五年半,意外发芽怎么办?
- 发表评论
-
- 最新评论 进入详细评论页>>
- 推荐内容
-
- 大脑GABA受体可作为抑郁症和认识障
抑郁症是一种复杂的疾病,与大脑功能和机制的多种差异有关。...
- 老年性痴呆,可不仅仅是记性差!
第一大征兆:记忆力衰退 记忆力衰退,尤其是对近期事物的遗忘...
- 《自然》:阿尔兹海默传染假说新
要说哪种疾病最可怕,奇点糕觉得还是 阿尔兹海默 病(Alzheimer...
- PNAS:一晚上不睡竟然会增加患阿尔
仅仅经历一晚上没有 睡 觉就会让人们大脑中淀粉样蛋白快速明...
- 保护大脑的“力量”抵御阿尔茨海
有史以来第一次,非传染性慢性病(癌症、心脏病、糖尿病和痴呆...
- 细菌真地也会在我们的大脑中安家
我们知道肠道中的 细菌 群体对我们的健康有很大的影响。这些...
- 大脑GABA受体可作为抑郁症和认识障
 通俗意义上的“合体”,大概就是这么一回事。图片来源:tumblr.com
通俗意义上的“合体”,大概就是这么一回事。图片来源:tumblr.com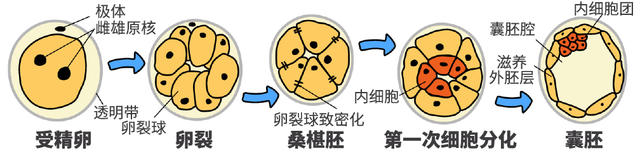 哺乳动物早期胚胎发育过程。我们每一个生命体都来自于一个叫做“受精卵”(zygote)的全能细胞,随后,这个巨大的细胞便会一分二,二分四,形成一个包含数十个卵裂球的“桑椹胚”(Morula),在桑椹胚阶段,胚胎发生第一次细胞分化,并产生一个腔隙而形成囊胚。原图来源:wikipedia.org/
哺乳动物早期胚胎发育过程。我们每一个生命体都来自于一个叫做“受精卵”(zygote)的全能细胞,随后,这个巨大的细胞便会一分二,二分四,形成一个包含数十个卵裂球的“桑椹胚”(Morula),在桑椹胚阶段,胚胎发生第一次细胞分化,并产生一个腔隙而形成囊胚。原图来源:wikipedia.org/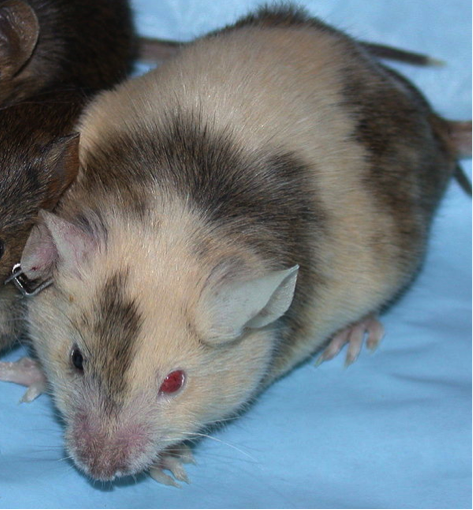 黑白小鼠胚胎“合体”后得到的嵌合体小鼠。图片来源:wikipedia.org
黑白小鼠胚胎“合体”后得到的嵌合体小鼠。图片来源:wikipedia.org 胚胎干细胞学的开创者马丁·埃文斯爵士。图片来源:wikipedia.org
胚胎干细胞学的开创者马丁·埃文斯爵士。图片来源:wikipedia.org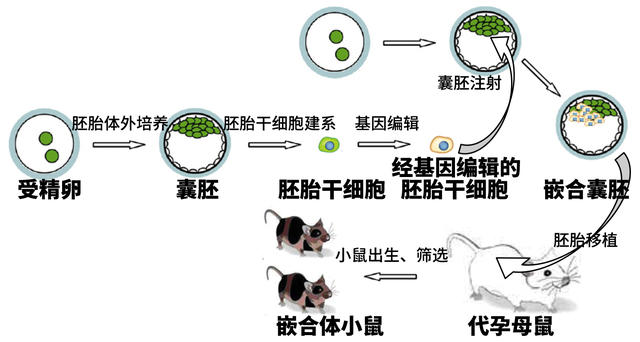 用处巨大的“合体”。图为利用嵌合体技术编辑小鼠基因的一般流程。图片来源:鬼谷藏龙
用处巨大的“合体”。图为利用嵌合体技术编辑小鼠基因的一般流程。图片来源:鬼谷藏龙 世界首个完成灵长类胚胎干细胞体外培养的科学家詹姆斯·汤姆森。图片来源:wikipedia.org
世界首个完成灵长类胚胎干细胞体外培养的科学家詹姆斯·汤姆森。图片来源:wikipedia.org