|
来源︱Wiley神经心理 责编︱王思珍 编辑︱杨彬伟
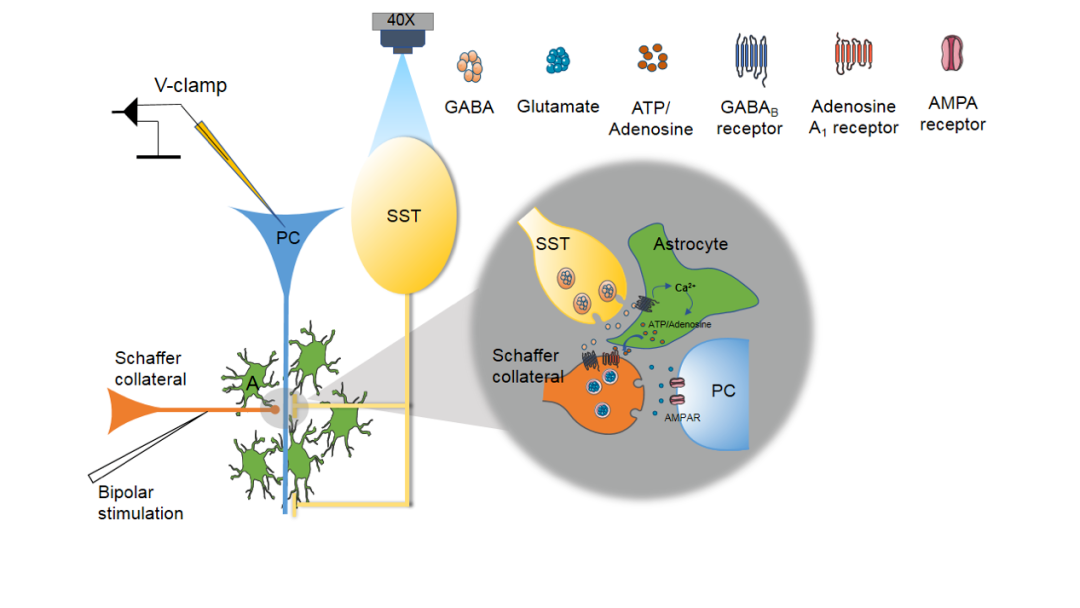
大量研究证实GABA ergic神经元通过激活突触前GABAB受体(GABABRs)来调节突触兴奋性。然而,最近的研究表明星形胶质细胞也表达GABABRs并能对GABAergic神经元活动作出反应。但是,上述关于GABA ergic神经元通过GABABRs调节突触兴奋性的相关机制中,研究者很难区分或者忽略了星形胶质细胞GABABRs是否参与了此过程。 2022年7月1日,浙大城市学院医学院曾玲晖教授和沈伟达老师合作在Journal of Neurochemistry杂上以OriginalArticle的形式发表了题为Somatostatin interneurons inhibit excitatory transmission mediated by astrocytic GABABand presynaptic GABABand adenosine A1receptors in the hippocampus的研究论文,运用全细胞膜片钳记录、光遗传学、钙成像和药理学等技术证实了生长抑素中间神经元(SOM-INs)通过星形胶质细胞GABABRs参与兴奋性突触调节并揭示了其内在机制。
GABAergic中间神经元对于协调大脑内的兴奋模式和同步神经元网络活动至关重要。其中,表达生长抑素(SOM)的中间神经元是一种靶向锥体神经元远端树突区域的中间神经元,其释放的GABA作用于兴奋性突触前GABAB受体(GABABRs)起到抑制突触传递的作用。 星形胶质细胞通过其表达的多种膜受体感知周围的变化。已有报道证实GABAergic中间神经元的活动可诱导星形胶质细胞释放ATP/Adenosine,从而激活突触前Adenosine A1受体(A1R)并抑制兴奋性突触传递。然而,尚不清楚哪种类型的中间神经元参与了这些过程。此外,最近的研究结果表明,SOM-INs激活可增强星形胶质细胞中的Ca2+信号。因此作者推测,星形胶质细胞GABABRs激活引起的嘌呤信号参与了SOM-INs介导的兴奋性突触传递的调节。 为了证明作者的猜想,作者通过脑立体定位注射病毒的方法,使海马区SOM-INs表达光敏蛋白ChR2。作者发现蓝光刺激SOM-INs能引起CA3-CA1兴奋性突触传递减弱,并且这种现象能被GABABRs阻断剂阻断,提示GABABRs参与了此过程(图1)。
图1GABAB受体参与光遗传学激活SOM-INs引起的兴奋性突触传递抑制 (图源:Shen W,et al.,Journal of Neurochemistry,2022)
接下来,作者通过光遗传和Ca2+成像相结合的方法发现,蓝光激活SOM-INs时能引起星形胶质细胞Ca2+信号增强,后期通过药理学实验发现星形胶质细胞GABABRs介导了此过程(图2)。
图2SOM-INs通过激活GABABRs引起星形胶质细胞胞内Ca2+信号增强 (图源:Shen W,et al.,Journal of Neurochemistry,2022)
随后,作者通过星形胶质细胞Ca2+浓度钳制实验证实了星形胶质细胞参与了SOM-INs兴奋引起的突触传递减弱现象(图3)。
图3星形胶质细胞Ca2+信号参与SOM-INs激活引起的兴奋性突触抑制 (图源:Shen W,et al.,Journal of Neurochemistry,2022)
最后,作者通过药理学和电生理等技术,解析出星形胶质细胞释放的递质(ATP/Adenosine)通过作用于突触前A1R参与了此过程(图4)。
图4SOM-INs 通过星形胶质细胞介导的ATP/Adenosine信号作用于突触前A1R抑制突触传递 (图源:Shen W,et al.,Journal of Neurochemistry,2022)
图5 工作总结图:海马SOM-INs调控兴奋性突触传递的信号通路示意图 (图源:Shen W,et al.,Journal of neurochemistry,2022)
研究结果表明,SOM-INs释放的GABA能作用于星形胶质细胞GABABRs引起星胶胞内Ca2+信号的升高。此外,作者还发现星形胶质细胞GABABRs激活引起的Ca2+信号升高能诱导星形胶质细胞释放ATP/Adenosine,ATP/Adenosine作用于突触前A1R抑制海马CA3-CA1通路的突触传递。该研究为SOM-INs调控突触传递的机制提供了一个全新的视角。 浙大城市学院医学院曾玲晖教授和沈伟达老师为本文的共同通讯作者。浙大城市学院和浙江大学联培研究生李紫荆、唐烨姣和浙大城市学院本科生韩普凡为本文的共同第一作者。本研究工作得到了浙江省重点研发项目(20220C03034)和国家大学生创新创业训练计划项目(202213021026)等资金的资助。
(责任编辑:泉水) |
JNC︱曾玲晖团队揭示海马生长抑素中间神经元通
时间:2022-08-29 06:44来源:生物大咔 作者:叮咚 点击:
335次
顶一下
(0)
0%
踩一下
(0)
0%
------分隔线----------------------------
- 发表评论
-
- 最新评论 进入详细评论页>>
- 推荐内容
-
- Science Advance:光催化激活神经Ca2+信号
近日,杭师大材化学院刘俊秋教授团队/生科院沈万华教授团队携...
- 体生长抑素信号在大脑中的作用
作者:宾夕法尼亚州立大学 Sam Sholtis 新研究表明,由大脑中许多...
- 协和发现国内首例“阴性艾滋病患
HIV抗体检测为常见的艾滋病筛查手段,阳性一般意味着感染,阴...
- 研究发现:月圆之周自杀死亡人数
作者:印第安纳大学医学院 图片来源:Pixabay/CC0 公共领域 几个...
- 大脑图像的清晰度提高了 6400 万倍
杜克大学 超级强大的核磁共振成像与光片显微镜相结合,使研究...
- 研究发现:保持免疫复原力的人更
作者:德克萨斯大学圣安东尼奥健康科学中心 Sunil Ahuja、Muthu ...
- Science Advance:光催化激活神经Ca2+信号