|
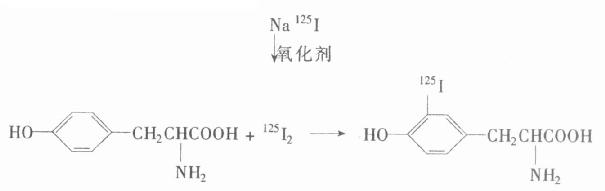
第二节 放射性碘标记 在RIA中,标记抗原质量的优劣,直接影响测定结果,必须制备比放射性强、纯度高的标记抗原,并保持免疫活性不受丧失。 一、同位素的选择 同位素有稳定性和放射性两种。放射性同位素可利用其衰变时放出的放射线进行测量,这种测量较灵敏而方便,故多用放射性同位素。标记抗原,常用的放射性同位素有3H、14C、131I和125I等。在使用上各有其优缺点,可根据所进行的放射免疫分析的类型特点,标记物制备和供应情况以及实验室设备条件等作适当的选择(表8-1)。大多数抗原分子中都含有C、H等原子,所以用14C或3H标记不改变抗原的结构及其免疫学活性,且14C、3H半衰期长,所标记的抗原长时间放置后仍可使用,这都是其优点。14C或3H标记的不足之处是操作较繁琐,并难以获得高比放射性的标记物;3H及14C放出的都是弱β射线,需用较昂贵的液体闪烁计数器方能获得较高效率的测量,且测定操作也较麻烦。但某些抗原用放射性碘标记容易丧失免疫化学或生物学活性者,则仍以采用3H或14C标记物为佳。 表8-1 标记抗原常用的放射性同位素及其性质 放射性元素 半衰期 射线种类及能量(百万电子伏特) β γ14 C 5720年 0.155 -3 H 12.5年 0.0189 - 125I 60天 - 0.035131 I 8.05天 0.608,0.335,0.250 0.364,0.637,0.722大多数抗原分子中是不含碘的,引入碘原子就改变了抗原的分子结构,往往容易损伤抗原的免疫化学活性;且放射性碘的半衰期较短,标记物放置后因衰变使放射性降低,因而需要经常制备标记物或要求能定期提供放射性碘标记都能适用,放射性碘放出γ—射线,用一般晶体闪烁计数器就能获得较高效率而精确的测量,测量操作也很简单。由于这些突出的优点,目前在放射免疫分析中,使用放射性碘标记物最多。 从应用角度来看,131I和125I又各有其优缺点,可根据实验的要求、仪器的条件和放射性碘制剂的规格等条件合理选用。但相对而言,125I有较多的优点,一是半衰期适中,允许标记化合物的商品化及贮存应用一段时间;二是它只发射28keV能量的X射线和35keV能量的γ射线,而无β粒子,因而辐射自分解少,标记化合物有足够的稳定性。放射性碘适用于放射免疫分析许多对象(包括蛋白质、肽类、固醇类、核酸类以及环型核苷酸衍生物等)的标记,且操作简单,一般实验室都不难做到。 二、蛋白质与多肽激素的放射性碘标记 要制备高比度、高纯度与免疫化学活性好的标记物,首先要有高纯度、良好免疫活性的抗原。用作放射标记加网免疫分析的特异性,所以若用纯度不高的抗原作标记,则标记后必须采取适当的步骤除去杂质,以获得高纯度的标记物。标记对象的纯化应尽量采用温和的方法,否则在纯化操作中已受潜在性损伤的蛋白质(这时表面上活性可能还是良好的),再经标记反应时所受的损伤,活性就会显著降低,影响以后的放射分析结果。有了好的纯抗原,还要采用适当方法加以标记,尽量获取高比放射性、而又能保持良好的特异免疫化学活性的标记物。这些都是放射免疫分析能取得高特异性和高灵敏度的关键问题。 多肽激素与蛋白质多用碘标记,最常用的是125I。碘化反应的基本过程如下:通过氧化剂的作用,使碘化物(125I-)氧化成的碘分子(125I2),再与多肽激素、蛋白质分子中的酪氨酸残基发生碘化作用。所以不管采用哪一种放射性碘标记法,标记的化合物内部必须有碘原子可结合的基团,即结构上要含有酪胺基或组织胺残基。凡蛋白质、肽类等抗原,在结构上含有上述基团的可直接用放射性碘进行标记。如不含上述基团的,放射性碘无法标记,必须在这些化合物的结构上连接上述基团后才能进行碘标记。 因此影响蛋白质、多肽碘化效率的因素,主要决定于蛋白质、多肽分子中酪氨酸残基的数量及它们在分子结构中暴露的程度;此外,碘化物的用量、反应条件(pH、温度、反应时间等)及所用氧化剂的性质等也有影响。 常用的标记方法有: (一)氯胺T法 氯胺T法标记效率高、重复性好、试剂便宜易得,是目前使用最多的碘标记方法。 1.原理氯氨—T(Chloramine--T)是一种温和的氧化剂,在水溶液中产生次氯酸,可使碘阴离子氧化成碘分子。这活性碘可取代肽链上酪氨酸苯环上羟基位的一个或两个氢,使之成为含有放射性碘化酪氨酸的多肽链。
2.方法以125I—AVP的制备为例。 (1)碘化反应:AVP5μg+0.5mol/l PB50μl(pH7.5)+1251800μCi,混合后,加入新配置的Ch—t 30μg/15μl(0.05mol/l PB, pH7.5)。迅速振荡混匀,室温下反应40s。 (2)终止碘化反应:加入还原剂偏重亚硫酸钠40μg/20μl(0.05mol/l PB, pH7.5),以终止碘化反应。 (3)Bio—Gel P2层析纯化:将碘化反应混合液注入Bio—Gel P2柱,用0.1n HAC溶液洗脱,分部收集,每2min收集一管,共收集60管。 (4)放射性测量:测定各收集管的放射性,出现两个峰,第一峰为125I—AVP,第二峰为游离碘盐峰。第一个峰中计算最高的几管,留下备用。 为了解标记抗原的质量,每次碘标记后应计算出碘的利用率,标记上多少放射性碘,以及每微克抗原结合上多少放射性碘。 (5)标记抗原的贮存:经纯化与检查后的标记物、加入1/8体积的异丙醇,分成若干小份,置于铅罐中,在-20℃以下的冰箱中贮存备用,应避免反复冻融。标记抗原在贮存中是不稳定的,这是因为:一是脱碘,标记的碘从原来位置上脱落,变成游离碘;二是蛋白损伤、变性,成为聚合大分子或断键成小分子碎片。由于上述原因,使B/F明显降低,标准曲线斜率变小,以致不能使用,故需分离纯化,其方法是用Sephadex G100长柱(40~80cm )过柱,洗脱后出现3个峰。第1个峰分子量大,是蛋白变性的聚合的大分子,尚保留部分抗原决定簇,免疫活性弱;第2个峰是纯抗原的蛋白峰,免疫活性好;第3个峰是游离125I或小分子碎片,不具备免疫活性。收集到的第2个纯抗原蛋白峰,免疫活性好;第3个峰是游离125I或小分子碎片,不具备免疫活性。收集到的第2个纯抗原蛋白峰,其性能类似于新鲜标记的抗原。分离纯化的方法解决了标记抗原的贮存、长期使用问题,特别对来之不易的抗原更显得重要。 2.注意事项 (1)放射性碘源的选用:无载体的131I或125I均可用于碘化标记,但应尽量选用新鲜的、比放射强度高的、含还原剂量少的放射性碘源。碘源的比放射强度最好≥50~100mCi/ml,至少也要>30mCi/ml,否则加入碘源的容量要增加,随着带入碘源中含有的还原剂(为放射性碘源运输保存所需加入)量也增加,这将会显著降低碘利用率及标记蛋白比放射强度。放置较久和放射性碘源,一方面因衰变致比放射强度降低,另一方面因水的辐射化学产物增多(主要是131I源),都会降低标记时的碘利用率。放射性碘源含还原剂(如Na2S2O5等)量多时,会抵消氯胺T的作用,降低碘利用率,甚至导致标记完全失败。放射性碘源要用无载体的,标记所用全部用具和试剂必须不含碘;只要有极少量的碘的污染,非放射性碘就会稀释放射性碘,使放射性碘利用率显著降低。为了便于放射性防护和除污染,以及减少射线对蛋白质分子的损伤,标记投入的放射碘量不宜过大,一般以<5mCi为宜。 (2)放射性碘与多肽、蛋白质用量的比例:这比例对标记结果的影响很大。如上述原因,一般标记时放射性投入量不宜过多,示踪实验室中常规每次只用1~2mCi,因而放射性碘与多肽、蛋白质用量的比值主要靠标记时投入的多肽、蛋白质用量来控制。当投入的放射碘量一定时,多肽、蛋白质用量多(即I/多肽、蛋白质比值低),能获得高碘利用率,但所得标记蛋白比放射强度低;相反多肽、蛋白质用量少(即I/多肽、蛋白质比值高),则碘利用率降低,但所得标记多肽、蛋白比放射性随此比值变化都有较大的变动;而当此比值<1后,则碘利用率再下降的幅率较小,标记多肽、蛋白比放射性也不会再增加多少。 (3)氯胺T与偏重亚硫酸钠的用量及碘化反应时间:氧化碘化标记法中,会导致失活的最主要原因是氧化还原。氯胺T是氧化剂,早期用氯胺T法作碘化标记时氯胺T用量都比较大,或碘化反应时间较长,结果导致蛋白质结构和活性的严重损伤。氯胺T用量大,或长时间进行碘化反应,结果并不能使碘利用率和标记多肽、蛋白质比放射强度提高多少,反而使标记多肽、蛋白活性下降。当用不含还原剂或还原剂很少的放射性碘源时,试以各种蛋白质(包括白蛋白、球蛋白、ACTH、胰岛素等)作微量标记,当氯胺T用量为20μg/0.1ml反应液、0~20。C反应20s,碘利用率都已接近或达到最大峰,再加大氯胺T用量和延长反应时间是没有必要的。随放射性碘源中还原剂增多,氯胺T用量也应增加,以达到预期的碘利用率,但决不应盲目加大氯胺T用量和延长碘化反应时间(通常反应时间不要超过1min),否则会导致标记多肽、蛋白质严重失活,不能用于实验。当然,减少氯胺T用量要在了解放射性碘源还原剂含量的基础上,否则碘源中还原剂量较多,双盲目减少氯胺T用量,就会使标记失败。一般用125I标记时,氯胺T用量要适当加大。加入氯胺T后必须迅速混匀,以防标记不均匀。氯胺T与偏重亚硫酸钠溶液要新配制的。 氯胺T用量减少了,Na2S2O5用量也就可以随之减少。为保证按时终止碘化反应,实验时加入Na2S2O5一般都是过量的。氯胺T用量大时,加入Na2S2O5的剩余量也就会随之增加,这就可能加重某些对还原剂敏感的蛋白质或多肽生物活性的损伤。为此,Na2S2O5用量也不应过多。只要药品没有变质、试剂是新配的,以重量计算Na2S2O5加入量与氯胺T相同就足以保证终止碘化反应(按反应克分子浓度计算,Na2S2O5/氯胺T重量比约0.4),不要盲目加大用量,并应迅速将标记多肽、蛋白质从反应液中分离出来,以尽量减少多肽、蛋白质活性的损伤。 某些蛋白质或多肽对氯胺T较敏感,还可进一步减少氯胺T用量、缩短碘化反应时间、降低反应温度,以保护蛋白质的活性。这对一些较容易丧失活性蛋白质或多肽的碘标记十分重要。 (4)碘化反应体积:系指加入Na2S2O5终止反应前液体的总量。碘化反应体积愈小,局部反应物浓度愈高,所得碘利用率和标记多肽、蛋白比放射强度就愈高。所以,标记应采用比放射标记效果。当反应液量少(<0.2~0.3ml)时,反应体积对碘利用率和标记多肽、蛋白质比放射强度的高低影响较大;当反应液量大(>0.5~1.0ml)时则影响较小。微量氯胺T法放射碘标记时,一般多控制碘化反应体积<100μl。 (责任编辑:泉水) |
第二节 放射性碘标记
时间:2006-06-25 14:12来源:大众医药网 作者:admin 点击:
281次
顶一下
(9)
100%
踩一下
(0)
0%
------分隔线----------------------------
- 发表评论
-
- 最新评论 进入详细评论页>>