|
第十五章 醛、酮、醌 醛、酮和醌的分子构造中都含有相同的官能团—羰基 第一节 醛和酮 一、醛和酮的构造 羰基与一个氢原子和一个烃基相连的化合物叫做醛(甲醛例外,它的,羰基与两个氢原子相连),可用通式表示 羰基与两个烃基相连的化合物叫做酮,可用通式 羰基中的碳原子为sp2杂化,其中一个sp2杂化轨道与氧原子的一个p轨道按轴向重叠形成σ键;碳原子未参与杂化的p轨道与氧原子的另一个p轨道平行重叠形成π键。因此,羰基碳氧双键是由一个σ键和一个π键组成的。 由于氧原子的电负性比碳原子大,因此羰基中π电了云偏向于氧原子一边,使羰基碳原子带有部分正电荷,而氧原子则带有部分负电荷。羰基的极化情况可表示如下:
二、醛和酮的命名 (一)普通命名法 简单的脂肪醛按分子中的碳原子的数目,称为某醛。例如:
(二)系统命名法 对构造比较复杂的醛、酮则用系统命名法命名。命名时先选择包括羰基碳原子在内的最长碳链作主链,称为某醛或某酮。从醛基一端或从靠近酮基一端开始把主链中碳原子编号。由于醛基一定在碳链的链端,故不必用数字标明其位置,但酮基的位置必须标明,写在酮名的前面。主链上如有支链或取代基,应标明位次,把它的位次(按次序规则)、数目、名称写在某醛、某酮的前面。主链中碳原子的编号也可以用希腊字母表示,即把与羰基碳直接相连的碳原子用α表示,其它碳原子依次为β,γ…
三、醛、酮的物理性质 在常温下,除甲醛是气体外,12个碳原子以下的脂肪醛、酮都是液体,高级脂肪醛、酮和芳香酮多为固体。 由于醛或酮分子之间不能形成氢键,没有缔合现象,故它们的沸点比相对分子质量相近的醇低。但由于羰基的极性,增加了分子间的引力,因此沸点较相应的烷烃高。如表15-1所示。 表15-1 相对分子质量相近的烷、醇、醛、酮的沸点 名称 正戊烷 正丁醇 丁醛 丁酮 相对分子质量 72 74 72 72 沸点/℃ 36.1 117.7 74.7 79.6醛、酮羰基上的氧可以与水分子中的氢形成氢键,因而低级醛、酮(如甲醛、乙醛、丙酮等)易溶于水,但随着分子中碳原子数目的增加,它们的溶解度则迅速减小。醛和酮易溶于有机溶剂。一些醛、酮的物理常数见表15-2。 表15-2一些醛、酮的物理常数 名称 构造式 熔点/℃ 沸点/℃ 相对密度 溶解度g·(100H2O)-1 甲醛 HCHO -92 -19.5 0.815 55 乙醛 CH3CHO -123 20.8 0.781 溶 丙醛 CH3CH2CHO -81 48.8 0.807 20 丁醛 CH3CH2CH2CHO -97 74.7 0.817 4 乙二醛
四、醛、酮的化学性质 醛、酮的化学性质主要决定于羰基。由于构造上的共同特点,使这两类化合物具有许多相似的化学性质。但是醛与酮的构造并不完全相同,使它们在反应性能上也表现出一些差异。一般说来,醛比酮活泼,有些反应醛可以发生,而酮则不能。 (一)羰基的加成 同碳碳双键一样,羰基中的碳氧双键也是由一个σ键和一个π键所组成,所以醛、酮都易发生加成反应。但和烯烃的亲电加成不同,羰基的加成属于亲核加成。由于氧原子的电负性大于碳原子,使羰基发生极化,氧原子带有部分负电荷,碳原了带有部分正电荷。一般说来,带负电荷的氧比带正电荷的碳较为稳定。所以,当羰基化合物发生加成反应时,首先是试剂中带负电荷的部分加到羰基的碳原子上,形成氧带负电荷的中间体,然后试剂中带正荷部分加到带负虵荷的氧上。这种由亲核试剂(能提供电子对的试剂)进攻而引起蝗加成反应叫做亲核加成反应。这类加反应可用于下式表示:
醛及脂肪族甲基酮与氢氰酸作用,生成α-α羰基腈。
对于同一种亲核试剂,亲核加成的难易取决于羰基碳原子所带正电荷的强弱及位阻效应的大小。所谓位阻效应是指分子中相邻的原子或原子团,在空间所占的体积和位置而产生的影响。羰基碳原子所带正电荷越多,反应越容易进行;羰基上连接的烃基越大则位阻效应越大,亲核试剂就越不容易靠近,反应也就越不容易进行。酮的羰基和两个烃基相连,由于烷基的斥电子作用,降低了羰基碳原子的正电荷;另一方面酮的两上烃基增大了位阻效应,所以在许多亲核加成反应中,酮一般不如醛活泼。醛、酮亲核加成反应活泼性顺序排列如下:
醛、脂肪族甲基酮和低级环酮(成环的碳原子在8个以下)都能与过量的饱和亚硫酸氢钠溶液发生加成反应,生成稳定的亚硫酸氢盐中成物。
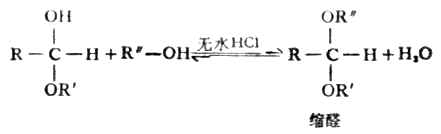
其它脂肪酮或芳香酮(包括芳香族甲基酮)由于受位阻效应的影响难以进行这种加成反应。 3.加醇 醛与醇在干燥氯化氢的催化下,发生加成反应,生成半缩醛。
|
第十五章 醛、酮、醌- -第一节 醛和酮
时间:2006-07-01 21:42来源:大众医药网 作者:admin 点击:
394次
顶一下
(10)
100%
踩一下
(0)
0%
------分隔线----------------------------
- 发表评论
-
- 最新评论 进入详细评论页>>
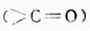 ,因而统称为羰基化合物。它们在性质上有很多相似的地方。许多醛和酮是重要的工业原料,有些是香料或重要药物。
,因而统称为羰基化合物。它们在性质上有很多相似的地方。许多醛和酮是重要的工业原料,有些是香料或重要药物。
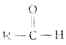 。
。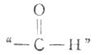 ”称为醛基,是醛的官能团,可简写为-CHO,它位于碳链的一端。
”称为醛基,是醛的官能团,可简写为-CHO,它位于碳链的一端。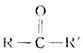 表示。酮的官能团
表示。酮的官能团 称为酮基,位于碳链中间。在一元酮中,两个烃基相同的叫单酮,两个烃基不同的叫做混酮。
称为酮基,位于碳链中间。在一元酮中,两个烃基相同的叫单酮,两个烃基不同的叫做混酮。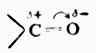
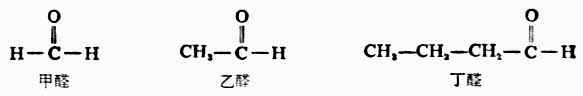 简单的酮可按羰基所连接的两上烃基命名。例如:
简单的酮可按羰基所连接的两上烃基命名。例如:

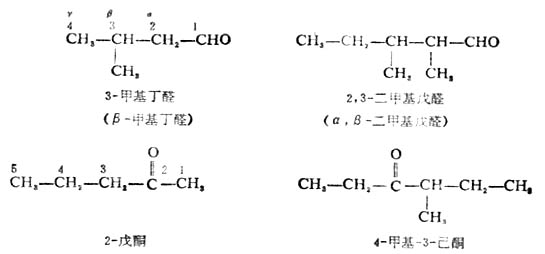 命名不饱和醛、酮则需标出不饱和键和羰基的位置。
命名不饱和醛、酮则需标出不饱和键和羰基的位置。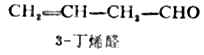 多元醛、酮命名时,同样选择包括羰基碳原子在内的最长碳链作为主链,编号时使羰基位置数字最小,同时加上用汉字数字表示的羰基数目。
多元醛、酮命名时,同样选择包括羰基碳原子在内的最长碳链作为主链,编号时使羰基位置数字最小,同时加上用汉字数字表示的羰基数目。
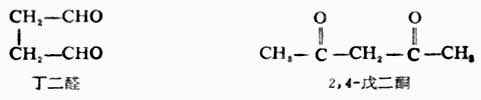 芳香醛、酮的命名,是以脂肪醛、酮为母体,芳香烃基作为取代基。
芳香醛、酮的命名,是以脂肪醛、酮为母体,芳香烃基作为取代基。

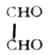 15
50.4
1.14
溶
丙烯醛
CH2=CHCHO
-87.7
53
0.841
溶
苯甲醛
15
50.4
1.14
溶
丙烯醛
CH2=CHCHO
-87.7
53
0.841
溶
苯甲醛
 -26
179
1.046
0.33
丙酮
CH3COCH3
-95
56
0.792
溶
丁酮
CH3COCH2CH3
-86
79.6
0.805
35.3
2-戊酮
CH3COCH2CH2CH3
-77.8
102
0.812
几乎不溶
3-戊酮
CH3CH2COCH2CH3
-42
102
0.814
4.7
环己酮
-26
179
1.046
0.33
丙酮
CH3COCH3
-95
56
0.792
溶
丁酮
CH3COCH2CH3
-86
79.6
0.805
35.3
2-戊酮
CH3COCH2CH2CH3
-77.8
102
0.812
几乎不溶
3-戊酮
CH3CH2COCH2CH3
-42
102
0.814
4.7
环己酮
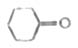 -16.4
156
0.942
微溶
4-甲基-3-戊烯-2-酮
(CH3)2C=CHCOCH3
-59
130
0.865
溶
丁二酮
-16.4
156
0.942
微溶
4-甲基-3-戊烯-2-酮
(CH3)2C=CHCOCH3
-59
130
0.865
溶
丁二酮
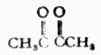 -2.4
88
0.980
25
2,4-戊二酮
-2.4
88
0.980
25
2,4-戊二酮
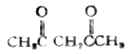 -23
138
0.792
溶
苯乙酮
-23
138
0.792
溶
苯乙酮
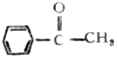 19.7
202
1.026
微溶
二苯甲酮
19.7
202
1.026
微溶
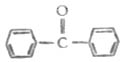
二苯甲酮
 48
306
1.098
不溶
48
306
1.098
不溶
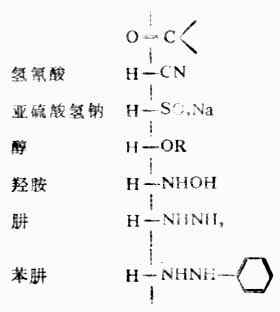
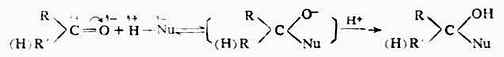 醛和酮可以与氢氰酸、亚梳酸氢钠、醇、氨的衍生物(如羟胺、肼等)试剂起加成反应。在反应产物中都是试剂中的氢与羰基上的氧相连接,其余部分与羰基的碳相连。
醛和酮可以与氢氰酸、亚梳酸氢钠、醇、氨的衍生物(如羟胺、肼等)试剂起加成反应。在反应产物中都是试剂中的氢与羰基上的氧相连接,其余部分与羰基的碳相连。
 1.加氢氰酸
1.加氢氰酸
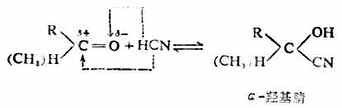 从上面的反应式或以看出,生成物比反应物增加了一个碳原子,因此这个反应可用来增长化合物的碳链。羟基腈在酸性水溶液中水解,即可得到羟基酸。
从上面的反应式或以看出,生成物比反应物增加了一个碳原子,因此这个反应可用来增长化合物的碳链。羟基腈在酸性水溶液中水解,即可得到羟基酸。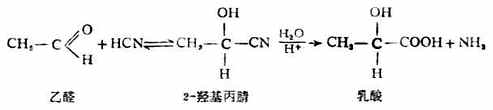 如果在醛、酮与氢氰酸反应中加入少量碱时,则反应速率明显加快;但如果加入酸,则抑制反应的进行。其原因是氢氰酸是一个弱酸,其离解过程为:
如果在醛、酮与氢氰酸反应中加入少量碱时,则反应速率明显加快;但如果加入酸,则抑制反应的进行。其原因是氢氰酸是一个弱酸,其离解过程为:
 在上述平衡体系中加入酸, 能HCN的离解,加入碱则促进HCN的离解,使CN-浓度增大。碱能加速羰基与氢氰酸的加成反应表明,氢氰 酸不是以分子,而是以CN-及H+参加反应的。又因碱的加入,能增加CN-的浓度,所以首先向羰基进攻的是CN-。这是亲核加成反应历程的实验基础。
在上述平衡体系中加入酸, 能HCN的离解,加入碱则促进HCN的离解,使CN-浓度增大。碱能加速羰基与氢氰酸的加成反应表明,氢氰 酸不是以分子,而是以CN-及H+参加反应的。又因碱的加入,能增加CN-的浓度,所以首先向羰基进攻的是CN-。这是亲核加成反应历程的实验基础。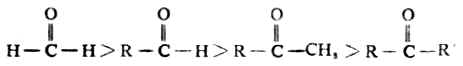 2.加亚硫酸氢钠
2.加亚硫酸氢钠
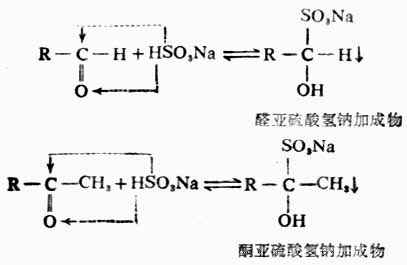 上述反应是可逆的。为使反应完全,常加入过量的饱和亚硫酸氢钠溶液,促使反应向右移动。由于这些加成物能被稀酸或稀碱分解成原来的醛或甲基酮,故常用这个反应来分离、精制醛或甲基酮。
上述反应是可逆的。为使反应完全,常加入过量的饱和亚硫酸氢钠溶液,促使反应向右移动。由于这些加成物能被稀酸或稀碱分解成原来的醛或甲基酮,故常用这个反应来分离、精制醛或甲基酮。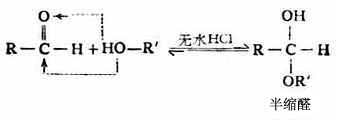
 (责任编辑:泉水)
(责任编辑:泉水)