|
日前,英国惠康基金会桑格研究所 (Wellcome Trust Sanger Institute) 的研究人员通过对乳腺癌患者的基因组突变特征的研究发现,将近有 20%的乳腺癌患者的基因缺陷与 BRCA1 或 BRCA2 基因突变造成的基因缺陷相似。这意味着这些患者可能从 PARP 抑制剂疗法中获益。这项研究发表在近期的《自然》子刊《Nature Medicine》上。 大约有 1~5%的乳腺癌患者携带 BRCA1 或 BRCA2 种系基因突变 (Germline Mutation) 。由于 BRCA 基因在细胞通过同源重组 (Homologous Recombination, HR) 修复 DNA 损伤方面起到重要作用,因此 BRCA 基因突变会导致细胞修复 DNA 损伤,特别是双链断裂方面水平下降。PRAP 抑制剂是特别设计出来治疗携带 BRCA 基因突变肿瘤的疗法。它的作用是进一步破坏细胞的其它 DNA 损伤修复机制,导致肿瘤细胞因为 DNA 损伤得不到修复而死亡。这种药物对因 BRCA 基因突变而导致同源重组功能缺失的癌细胞尤其有效。
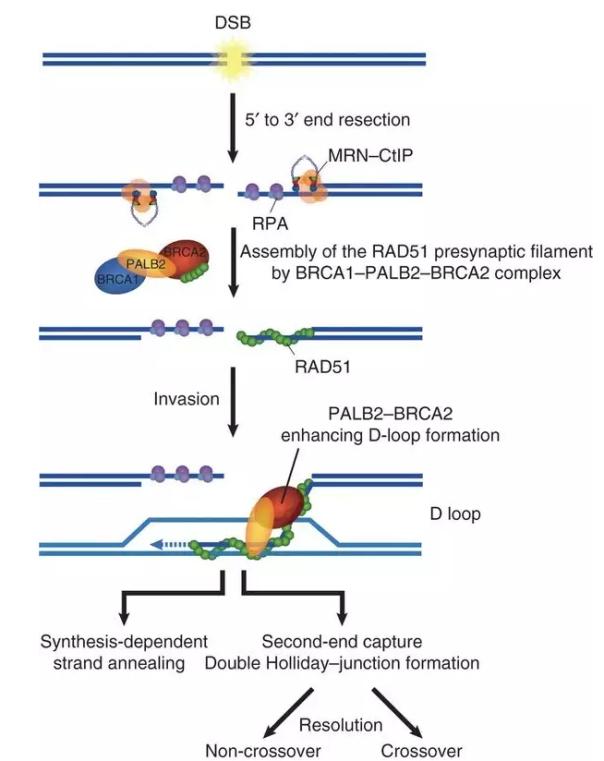
▲BRCA 参与同源重组 DNA 修复(图片来源:《Nature Structural & Molecular Biology》) 有很多肿瘤虽然不携带 BRCA 基因突变,但是由于其它原因导致细胞同源重组功能缺失,这些肿瘤也可以受益于 PARP 抑制剂疗法。因此,很多科研人员致力于找出肿瘤细胞中预测同源重组功能缺失的特征,希望能够根据这些特征找到那些可以获益于 PARP 抑制剂疗法的患者。 寻找这些基因特征的方法有两种,一种是从“因”的方向来找,查找那些会导致同源重组功能缺失的基因上的缺陷。这包括对所有已知与同源重组有关的基因进行测序以及对它们的启动子高甲基化 (Promoter Hypermethylation) 进行检测等等。而桑格研究所的研究人员所采用的策略是从“果”的方向来找。他们的想法是,如果肿瘤细胞中同源重组功能缺失,那么在基因组中会因为 DNA 修复功能下降而出现特定的基因突变特征。如果我们能够观察到这些基因突变特征,根据它们的存在就可以逆推出细胞的同源重组功能是否受到了损伤。
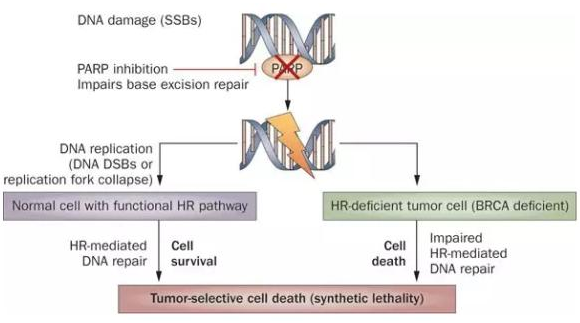
▲BRCA 缺陷与 PRAP 抑制剂的合成致死效应(图片来源:《Nature Reviews Clinical Oncology》) 为此,研究人员对 22 名携带 BRCA 种系基因突变的乳腺癌患者的肿瘤进行了全基因组测序,并且将这些肿瘤的基因组图谱与另一组从 235 名不含有 BRCA 种系基因突变的乳腺癌患者中获取的肿瘤基因组图谱进行比较。他们用这些基因组图谱数据训练一种计算机算法来找出携带 BRCA 种系基因突变的肿瘤在基因组水平上独特的基因变异特征,并且综合这些特征给出一个预测肿瘤同源重组功能缺失的参数。 当研究人员用这款称为 HRDetect 的计算机算法对 560 名乳腺癌患者的肿瘤基因组进行分析时,算法发现接近 20%患者的肿瘤有很大可能存在同源重组功能缺失。这个数字远远超过在 560 名患者中已知携带 BRCA 种系基因突变患者的数目。对这些患者的进一步审查发现其中很多患者携带着新的 BRCA 种系或体细胞基因突变,或者在 BRCA1 基因启动子区域存在高甲基化。 文章的资深作者,桑格研究所的 Serena Nik-Zainal 博士说:“过去 PRAP 抑制剂的临床试验大多聚焦在乳腺癌患者中 1~5%携带 BRCA 基因突变的那部分患者。我们的研究结果表明更多患者携带的肿瘤具有与携带 BRCA 基因突变患者的肿瘤相同的基因变异特征和弱点。我们应该探索这些患者是否能够从 PARP 抑制剂疗法中获益。” (责任编辑:泉水) |
Nature 子刊:20%的乳腺癌患者可受益于这一疗法
时间:2017-03-17 11:38来源:药明康德 作者:未知
顶一下
(0)
0%
踩一下
(0)
0%
------分隔线----------------------------
- 发表评论
-
- 最新评论 进入详细评论页>>
- 推荐内容
-
- 科学家在临床研究中开发出可杀死
美国最大的癌症研究和治疗机构之一希望之城(City of Hope)的研...
- 研究利用人体自身免疫细胞对抗脑
胶质母细胞瘤是最常见也是最致命的脑癌,它生长迅速,侵袭并...
- 科学家发现对50%癌细胞有效的细胞
斯坦福大学的科学家们发现了一种诱导癌细胞死亡的方法,这种...
- 超声波可能协助化疗药物通过血脑
破解脑癌治疗的密码可能要从破解大脑的保护罩开始。 大脑的大...
- 2018或将开启中国肿瘤免疫治疗新元
NGS作为一项重大的技术突破,从2010年前后开始肿瘤治疗的临床转...
- 新方法可提前诊断乳腺癌
癌症早期诊断对治疗非常重要。英国伦敦大学学院近日发表一项...
- 科学家在临床研究中开发出可杀死